Giải SBT KHTN 7 Kết nối tri thức bài 2 trang 7, 8, 9, 10, 11
Giải bài 2 nguyên tử trang 7, 8, 9, 10, 11 sách bài tập (SBT) Khoa học tự nhiên lớp 7 Kết nối tri thức. Bài 2.3. Trừ hạt nhân của nguyên tử hydrogen, hạt nhân các nguyên tử còn lại được tạo thành từ hạt.
Bài 2.1 trang 7 SBT KHTN lớp 7 - Kết nối tri thức
Phát biểu nào sau đây không mô tả đúng mô hình nguyên tử của Rơ-dơ-pho – Bo?
A. Nguyên tử có cấu tạo rỗng, gồm hạt nhân ở tâm nguyên tử và các electron ở vỏ nguyên tử.
B. Nguyên tử có cấu tạo đặc khít, gồm hạt nhân nguyên tử và các electron.
C. Electron chuyển động xung quanh hạt nhân theo những quỹ đạo xác định tạo thành các lớp electron.
D. Hạt nhân nguyên tử mang điện tích dương, electron mang điện tích âm.
Phương pháp:
- Nguyên tử có cấu tạo dạng rỗng.
- Nguyên tử có hạt nhân ở tâm mang điện tích dương, các electron mang điện tích âm, chuyển động xung quanh hạt nhân như các hành tinh quay xung quanh Mặt Trời.
Lời giải:
Đáp án đúng là: B
B không mô tả đúng vì nguyên tử có cấu tạo rỗng.
Bài 2.2 trang 7 SBT KHTN lớp 7 - Kết nối tri thức
Phát biểu nào sau đây không mô tả đúng vỏ nguyên tử theo mô hình nguyên tử của Rơ-dơ-pho – Bo?
A. Electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau tạo thành các lớp electron.
B. Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp electron khác có chứa tối đa 8 electron hoặc nhiều hơn.
C. Lớp electron trong cùng gần hạt nhân nhất có tối đa 8 electron, các lớp electron khác có chứa tối đa nhiều hơn 8 electron.
D. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
Phương pháp:
- Nguyên tử có cấu tạo dạng rỗng.
- Nguyên tử có hạt nhân ở tâm mang điện tích dương, các electron mang điện tích âm, chuyển động xung quanh hạt nhân như các hành tinh quay xung quanh Mặt Trời.
Lời giải:
Đáp án đúng là C.
C không mô tả đúng vì: Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp electron khác có chứa tối đa 8 electron hoặc nhiều hơn. Ví dụ:
+ Lớp thứ nhất có tối đa 2 electron.
+ Lớp thứ 2 có tối đa 8 electron.
+ Lớp thứ 3 có tối đa 18 electron.
Bài 2.3 trang 7 SBT KHTN lớp 7 - Kết nối tri thức
Trừ hạt nhân của nguyên tử hydrogen, hạt nhân các nguyên tử còn lại được tạo thành từ hạt
A. electron và proton.
B. electron, proton và neutron.
C. neutron và electron.
D. proton và neutron.
Phương pháp:
Lời giải:
Đáp án đúng là: D
Trừ hạt nhân của nguyên tử hydrogen, hạt nhân của các nguyên tử còn lại được tạo thành từ hạt proton và neutron.
Bài 2.4 trang 7 SBT KHTN lớp 7 - Kết nối tri thức
Cho các phát biểu:
(1) Nguyên tử trung hòa về điện.
(2) Khối lượng của nguyên tử tập trung chủ yếu ở hạt nhân.
(3) Trong nguyên tử, số hạt mang điện tích dương bằng số hạt mang điện tích âm nên số hạt electron bằng số hạt neutron.
(4) Vỏ nguyên tử, gồm các lớp electron có khoảng cách khác nhau đối với hạt nhân.
Trong các phát biểu trên, số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Phương pháp:
Lời giải:
Đáp án đúng là: C
Các phát biểu đúng là: (1); (2); (4).
Phát biểu (3) sai vì số hạt proton bằng số hạt electron.
Bài 2.5 trang 8 SBT KHTN lớp 7 - Kết nối tri thức
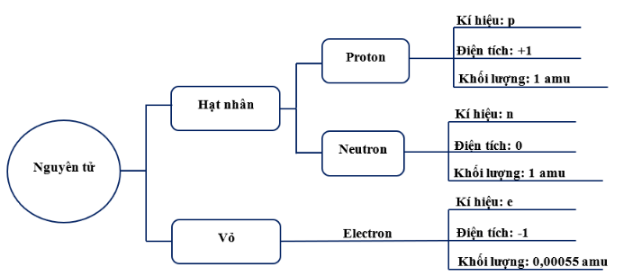
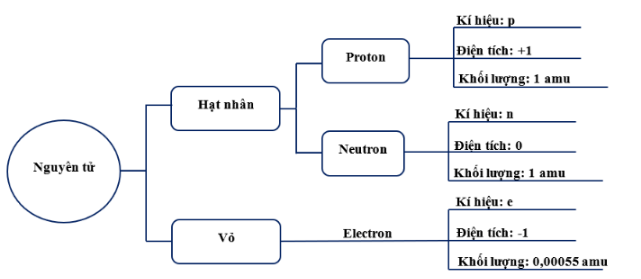
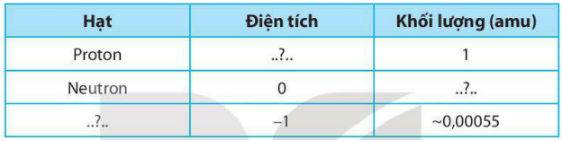
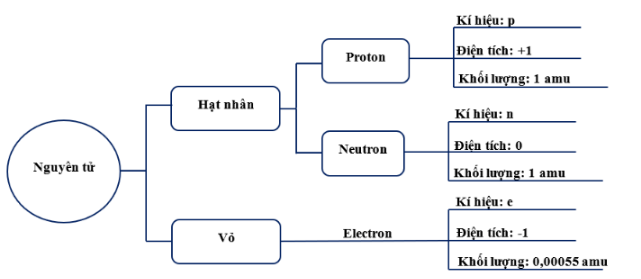
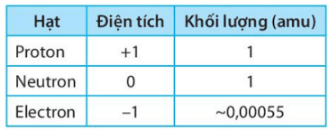
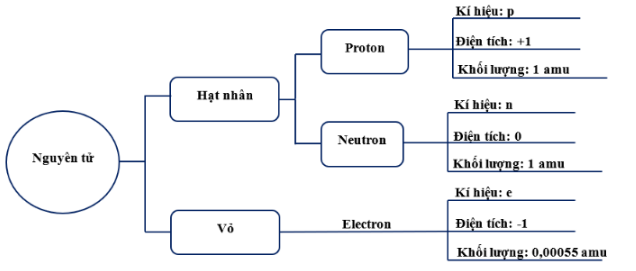
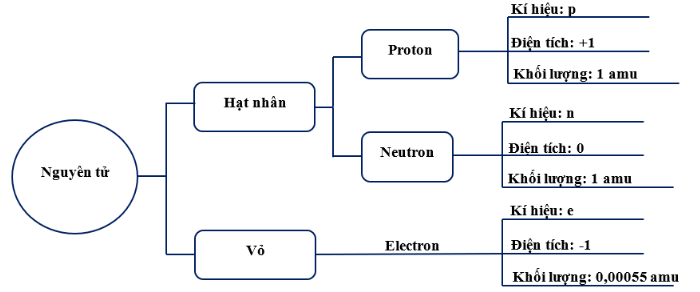
Hãy viết tên, điện tích và khối lượng của các hạt cấu tạo nên nguyên tử vào chỗ trống để hoàn thiện bảng dưới đây.
Phuơng pháp:
Lời giải:
Bảng tên, điện tích và khối lượng các hạt tạo nên nguyên tử:
Bài 2.6 trang 8 SBT KHTN lớp 7 - Kết nối tri thức
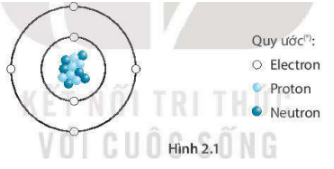
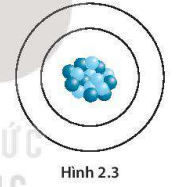
Từ Hình 2.1 mô phỏng một nguyên tử carbon, hãy cho biết trong một nguyên tử carbon có bao nhiêu hạt electron, proton, neutron.
Phương pháp:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Lời giải:
Quan sát Hình 2.1 xác định được, nguyên tử carbon có 6 electron, 6 proton và 6 neutron.
Bài 2.7 trang 8 SBT KHTN lớp 7 - Kết nối tri thức
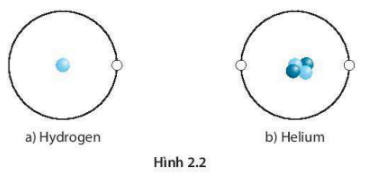
Mặt Trời chứa chủ yếu hai nguyên tố hóa học là hydrogen (H) và helium (He). Hình biểu diễn một nguyên tử hydrogen và một nguyên tử helium.
Dựa vào hình vẽ trên hãy cho biết:
a) Mỗi vòng tròn xung quanh hạt nhân được gọi là gì?
A. Một liên kết.
B. Một electron.
C. Một lớp vỏ electron.
D. Một proton.
b) Có bao nhiêu electron trong lớp vỏ của nguyên tử H, He? Có bao nhiêu proton trong hạt nhân của nguyên tử H, He?
Phương pháp:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn.
Lời giải:
a) Đáp án đúng là: C
Dựa vào hình vẽ, mỗi vòng tròn quanh hạt nhân biểu thị một lớp vỏ eclectron.
b) Nguyên tử H có 1 electron, 1 proton; nguyên tử He có 2 electron, 2 proton.
Bài 2.8 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
Giải thích vì sao có thể coi khối lượng nguyên tử tập trung ở hạt nhân, lấy ví dụ về một nguyên tử để minh họa.
Phương pháp:
Lời giải:
Nguyên tử được tạo thành từ 3 loại hạt là proton, electron và neutron. Khối lượng nguyên tử là tổng khối lượng các hạt có trong nguyên tử. Tuy nhiên, do khối lượng của electron nhỏ hơn khối lượng của proton và neutron rất nhiều nên có thể coi khối lượng của electron là không đáng kể so với khối lượng của nguyên tử. Hay nói các khác, có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
Ví dụ: Nguyên tử carbon có 6 electron, 6 proton và 6 electron.
Khối lượng của nguyên tử là: 6.0,00055 + 6.1 + 6.1 = 12,0033 (amu), xấp xỉ khối lượng hạt nhân là 12 amu.
Bài 2.9 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
Nguyên tử lithium có 3 proton.
a) Có bao nhiêu electron trong nguyên tử lithium?
b) Biết hạt nhân nguyên tử lithium có 4 neutron, tính khối lượng nguyên tử của lithium theo đơn vị amu.
Phương pháp:
Lời giải:
a) Số electron = số proton ⇒ Nguyên tử lithium có 3 electron.
Khối lượng nguyên tử lithium là: 4 + 3 = 7 (amu).
Bài 2.10 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
Mô tả sự khác nhau giữa cấu tạo một nguyên tử hydrogen và cấu tạo một nguyên tử helium.
Phương pháp:
- Dựa vào dữ kiện bài 2.7 trong sách bài tập để biết số proton và electron của nguyên tử hydrogen và helium.
- Lưu ý: có thể cho biết số neutron trong các nguyên tử hoặc không. Vì cùng một nguyên tố hóa học sẽ có những nguyên tử có cùng số proton nhưng khác số neutron (khái niệm về đồng vị hóa học).
Lời giải:
Một nguyên tử hydrogen có 1 electron ở vỏ nguyên tử và 1 proton ở hạt nhân nguyên tử.
Nguyên tử helium có 2 electron ở vỏ nguyên tử, hạt nhân nguyên tử gồm 2 proton và 2 neutron.
Bài 2.11 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
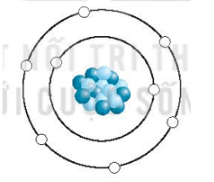
Oxygen là nguyên tố hóa học phổ biến trong không khí, duy trì sự sống và sự cháy. Hoàn thiện Hình 2.3 để mô tả cấu tạo một nguyên tử oxygen.
Phương pháp:
Phương pháp:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Lời giải:
Mô hình mô tả cấu tạo một nguyên tử oxygen:
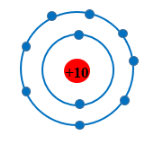
Bài 2.12 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
Một nguyên tử có 10 proton trong hạt nhân. Theo mô hình nguyên tử của Ro-dơ-pho – Bo, số lớp electron của nguyên tố đó là
A. 1.
B. 2.
C. 3.
D. 4.
Phương pháp:
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
- Vỏ nguyên tử gồm các electron sắp xếp thành từng lớp. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
Lời giải:
Đáp án đúng là: B
Ta có: số electron = số proton = 10.
Nguyên tử có 10 electron được phân bố vào 2 lớp (lớp thứ nhất có 2 electron, lớp thứ hai có 8 electron)
Trong một nguyên tử có số proton bằng 5, số electron trong các lớp của vỏ nguyên tử, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 1, 2, 8.
B. 2, 8, 1.
C. 2, 3.
D. 3, 2.
Phương pháp:
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: C
Nguyên tử có số proton = 5 ⇒ Số electron = 5.
Lớp electron bên trong, gần hạt nhân có 2 electron, lớp bên ngoài có 5 – 2 = 3 electron.
Bài 2.14 trang 9 SBT KHTN lớp 7 - Kết nối tri thức
Nitrogen là nguyên tố hóa học phổ biến trong không khí. Trong hạt nhân nguyên tử nitrogen có 7 proton. Số electron trong các lớp của vỏ nguyên tử nitrogen, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 7.
B. 2, 5.
C. 2, 2, 3.
D. 2, 4, 1.
Phương pháp:
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: B
Nguyên tử nitrogen có số electron = số proton = 7.
Lớp electron bên trong, gần hạt nhân có 2 electron, lớp bên ngoài có 7 – 2 = 5 electron.
Bài 2.15 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Trong hạt nhân nguyên tử fluorine có 9 proton. Số electron ở lớp ngoài cùng của vỏ nguyên tử fluorine là?
A. 2.
B. 5.
C. 7.
D. 8.
Phương pháp:
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: C
Nguyên tử fluorine có số electron = số proton = 9.
Lớp electron bên trong gần hạt nhân có 2 electron, lớp bên ngoài có 9 -2 = 7 electron.
Bài 2.16 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Nguyên tử calcium có 20 electron ở vỏ nguyên tử. Hạt nhân của nguyên tử có calcium có số proton là
A. 2.
B. 10.
C. 18.
D. 20.
Phương pháp:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Lời giải:
Đáp án đúng là: D
Calcium có số proton = số electron = 20.
Bài 2.17 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Nguyên tử aluminium có 13 electron ở vỏ. Số electron ở lớp trong cùng của nguyên tử aluminium là
A. 2.
B. 8.
C. 10.
D. 18.
Phương pháp:
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: A
Số electron ở lớp trong cùng của nguyên tử nhôm (aluminium) là 2.
Bài 2.18 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Muối ăn chứa hai nguyên tố hóa học là sodium và chlorine. Trong hạt nhân nguyên tử của các nguyên tố sodium và chlorine có lần lượt 11 và 17 proton. Số electron ở lớp ngoài cùng của vỏ nguyên tử sodium và chlorine lần lượt là
A. 1 và 7.
B. 3 và 9.
C. 9 và 15.
D. 3 và 7.
Phương pháp:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: A
- Nguyên tử natri có số electron = số proton = 11.
Lớp electron bên trong gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 11 – 8 – 2 = 1 electron.
- Nguyên tử chlorine có số electron = số proton = 17.
Lớp electron bên trong, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 17 – 8 – 2 = 7 electron.
Bài 2.19 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Trong hạt nhân nguyên tử sulfur có 16 proton. Số electron trong các lớp của vỏ nguyên tử sulfur, viết từ trong ra lớp ngoài, lần lượt là
A. 2, 10, 6.
B. 2, 6 8.
C. 2, 8, 6.
D. 2, 9, 5.
Phương pháp:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Đáp án đúng là: C
Nguyên tử lưu huỳnh (sulfur) có số electron = số proton = 16.
Lớp electron trong cùng, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 16 – 8 – 2 = 6 electron.
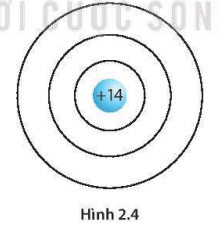
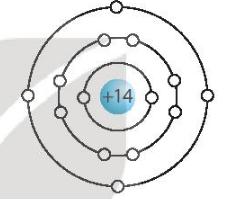
Bài 2.20 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
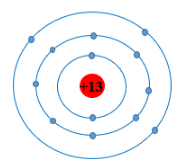
Trong hạt nhân nguyên tử của nguyên tố silicon có 14 proton, vỏ nguyên tử silicon có ba lớp electron. Hãy hoàn thiện hình 2.4 để mô tả mô hình một nguyên tử silicon.
Phương pháp:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
Lời giải:
Mô tả cấu tạo của một nguyên tử silicon:
Bài 2.21 trang 10 SBT KHTN lớp 7 - Kết nối tri thức
Hạt nhân một nguyên tử flourine có 9 proton và 10 neutron. Khối lượng của nguyên tử flourine xấp xỉ bằng
A. 9 amu.
B. 10 amu.
C. 19 amu.
D. 28 amu.
Phương pháp:
Khối lượng của một nguyên tử xấp xỉ bằng khối lượng của hạt nhân nguyên tử đó.
Lời giải:
Đáp án đúng là: C
Một cách gần đúng, coi khối lượng nguyên tử xấp xỉ bằng khối lượng của hạt nhân.
Khối lượng của nguyên tử fluorine = 9.1 + 10.1 = 19 (amu).
Bài 2.22 trang 11 SBT KHTN lớp 7 - Kết nối tri thức
Muối ăn chứa hai nguyên tố hóa học là sodium và chlorine. Trong hạt nhân nguyên tử của các nguyên tố sodium và chlorine có lần lượt 11 và 17 proton. Số electron trong các lớp của vỏ nguyên tử sodium và chlorine, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 2, 9 và 2, 10, 5.
B. 2, 9 và 2, 8, 7.
C. 2, 8, 1 và 2, 8, 7
D. 2, 8, 1 và 2, 8, 5.
Phương pháp:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn
- Vỏ nguyên tử gồm các electron sắp xếp thành từng lớp. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
Lời giải:
Đáp án đúng là: C
- Nguyên tử natri có số electron = số proton = 11.
Lớp electron bên trong gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 11 – 8 – 2 = 1 electron.
- Nguyên tử chlorine có số electron = số proton = 17.
Lớp electron bên trong, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 17 – 8 – 2 = 7 electron.
Sachbaitap.com
Bài viết liên quan
Các bài khác cùng chuyên mục
- Giải SBT KHTN 7 Kết nối tri thức bài 24 trang 57, 58, 59 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 23 trang 56, 57 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 22 trang 54, 55 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 21 trang 53, 54 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 20 trang 51, 52 (10/12)
- Bài 24. Thực hành: Chứng minh quang hợp ở cây xanh
- Bài 23. Một số yếu tố ảnh hưởng đến quang hợp
- Bài 22. Quang hợp ở thực vật
- Bài 21. Khái quát về trao đổi chất và chuyển hóa năng lượng
- Chương VII. Trao đổi chất và chuyển hóa năng lượng sinh vật
- Bài 20. Chế tạo nam châm điện đơn giản
- Bài 19. Từ trường
- Bài 18. Nam châm
- Chương VI. Từ
- Bài 17. Ảnh của vật qua gương phẳng
- Bài 22 Đọc mở rộng trang 111 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 22 Luyện viết đoạn văn thể hiện tình cảm, cảm xúc về một sự việc trang 111 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 22 Bộ đội về làng trang 109 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Viết đoạn văn nêu ý kiến tán thành một sự việc, hiện tượng (Bài viết số 2) trang 108 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Luyện tập về câu ghép trang 107 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Anh hùng lao động Trần Đại Nghĩa trang 106 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Đền ơn đáp nghĩa trang 104 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Đánh giá, chỉnh sửa đoạn văn nêu ý kiến tán thành một sự vật, hiện tượng trang 103 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Cụ Đồ Chiểu trang 101 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 19 Viết đoạn văn nêu ý kiến tán thành một sự việc, hiện tượng (Bài viết số 1) trang 100 SGK Tiếng Việt 5 Kết nối tri thức tập 2
 Tải app loigiaihay.com cho Android để lưu và xem mà không cần mạng!
Tải app loigiaihay.com cho Android để lưu và xem mà không cần mạng!