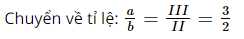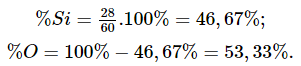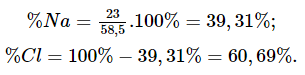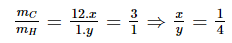Giải SBT KHTN 7 Kết nối tri thức bài 7 trang 26, 27, 28
Giải bài 7 hóa trị và công thức hóa trị trang 26, 27, 28 sách bài tập (SBT) Khoa học tự nhiên lớp 7 Kết nối tri thức. Bài 7.1.Đơn chất nitơ bao gồm các phân tử chứa hai nguyên tử nitơ. Công thức hóa học của đơn chất nitơ là
Xem thêm: Bài 7. Hóa trị và công thức hóa học
Bài 7.1 trang 26 SBT KHTN lớp 7 - Kết nối tri thức
Đơn chất nitơ bao gồm các phân tử chứa hai nguyên tử nitơ. Công thức hóa học của đơn chất nitơ là
A. N.
B. N2.
C. N2.
D. N2.
Lời giải:
Đáp án đúng là: C
Công thức phân tử của đơn chất nitơ là: N2.
Bài 7.2 trang 26 SBT KHTN lớp 7 - Kết nối tri thức
Một phân tử của hợp chất carbon dioxide chứa một nguyên tử carbon và hai nguyên tử oxygen. Công thức hóa học của hợp chất carbon dioxide là
A. CO2.
B. CO2.
C. CO2.
D. Co2.
Phương pháp:
+ Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo nên hợp chất kèm theo chỉ số ở chân bên phải của kí hiệu hóa học. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.
Lời giải:
Đáp án đúng là: A
Công thức hóa học của hợp chất carbon dioxide là CO2.
Bài 7.3 trang 26 SBT KHTN lớp 7 - Kết nối tri thức
Công thức hóa học của sodium hydroxide là NaOH. Hợp chất này chứa những nguyên tố hóa học nào? Trong một phân tử sodium hydroxide có bao nhiêu nguyên tử của mỗi nguyên tố đó?
Phương pháp:
- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.
Lời giải:
Hợp chất sodium hydroxide (NaOH) chứa các nguyên tố hóa học là Na, O và H. Trong một phân tử sodium hydroxide có 1 nguyên tử Na, 1 nguyên tử O và 1 nguyên tử H.
Bài 7.4 trang 26 SBT KHTN lớp 7 - Kết nối tri thức
Công thức của sulfuric acid là H2SO4.
a) Gọi tên các nguyên tố có trong sulfuric acid.
b) Có bao nhiêu nguyên tử của mỗi nguyên tố đó trong một phân tử sulfuric acid.
Phương pháp:
- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.
Lời giải:
a) Các nguyên tố hóa học có trong sulfuric acid: hydrogen; sulfur và oxygen.
b) Trong một phân tử sulfuric acid có 2 nguyên tử H, 1 nguyên tử S và 4 nguyên tử O.
Hãy viết công thức hóa học của các hợp chất sau đây:
a) Magnesium oxide, biết một phân tử của nó chứa một nguyên tử magnesium và một nguyên tử oxygen.
b) Copper sulfate, biết một phân tử của nó chứa một nguyên tử đồng, một nguyên tử sulfur và bốn nguyên tử oxygen.
c) Đường ăn, biết một phân tử của nó chứa 12 nguyên tử carbon, 22 nguyên tử hydrogen và 11 nguyên tử oxygen.
Phương pháp:
Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học
Lời giải:
a) Magnesium oxide có công thức hóa học là: MgO.
b) Copper sulfate có công thức hóa học là: CuSO4.
c) Đường ăn có công thức hóa học: C12H22O11.
Bài 7.6 trang 26 SBT KHTN lớp 7 - Kết nối tri thức
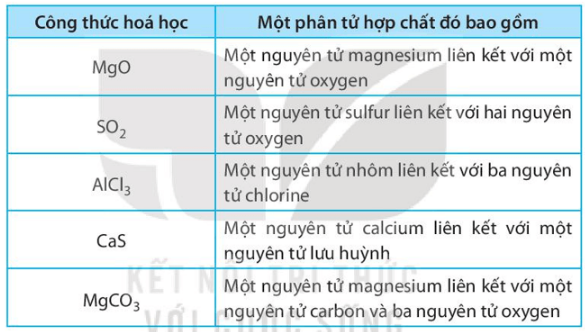
Điền công thức hóa học và mô tả số lượng các nguyên tử của các nguyên tố vào chỗ trống để hoàn thiện bảng sau:
Phương pháp:
Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học.
Để viết được công thức hóa học, cần phải nhớ được kí hiệu hóa học của nguyên tố.
Lời giải:
Bài 7.7 trang 27 SBT KHTN lớp 7 - Kết nối tri thức
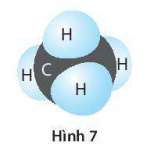
Hình 7 mô tả phân tử khí methane CH4.
a) Trong hợp chất này, nguyên tử C sử dụng bao nhiêu electron lớp ngoài cùng của nó để tạo liên kết cộng hóa trị với các nguyên tử H?
A. 2.
B. 4.
C. 8.
D. 10.
b) Cho biết mỗi một cặp electron dùng chung giữa các nguyên tử C và nguyên tử H tướng ứng với một liên kết cộng hóa trị, thì nguyên tử C tạo được bao nhiêu liên kết cộng hóa trị với các nguyên tử H?
A. 2.
B. 4.
C. 8.
D. 10.
Phương pháp:
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố (trừ helium) trong nhóm đó.
- Lớp electron ngoài cùng bền vững của khí hiếm là 8 electron (trừ helium). Nguyên tử của nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm gần nó nhất trong bảng tuần hoàn.
- Liên kết cộng hóa trị là liên kết được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung. Mỗi cặp electron dùng chung tạo nên một liên kết cộng hóa trị.
Lời giải:
a) Đáp án đúng là: B
Trong hợp chất CH4, nguyên tử C sử dụng 4 electron ở lớp ngoài cùng của nó để tạo các liên kết cộng hóa trị với các nguyên tử H.
b) Đáp án đúng là: B
Nguyên tử C tạo được 4 liên kết cộng hóa trị với các nguyên tử H.
Bài 7.8 trang 27 SBT KHTN lớp 7 - Kết nối tri thức
Hãy xác định hóa trị của các nguyên tố C, Si trong các hợp chất sau:
a) CCl4 biết trong hợp chất này Cl có hóa trị I.
b) SiO2, biết trong hợp chất này O có hóa trị II.
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
a) Gọi hóa trị của C là x ta có: x.1 = I.4 ⇒ x = IV.
Vậy C có hóa trị IV, trong hợp chất CCl4.
b) Gọi hóa trị của Si là y ta có: y.1 = II.2 ⇒ x = IV.
Vậy Si có hóa trị IV, trong hợp chất SiO2.
Bài 7.9 trang 27 SBT KHTN lớp 7 - Kết nối tri thức
Hãy viết công thức hóa học và gọi tên của hợp chất được tạo thành từ sự kết hợp giữa các đơn chất sau:
a) sắt và chlorine, biết trong hợp chất này sắt hóa trị III và chlorine hóa trị I.
b) natri và oxygen, biết natri hóa trị I và oxygen hóa trị II.
c) hydrogen và fluorine, biết hydrogen hóa trị I và fluorine hóa trị I.
d) kali và chlorine, biết kali hóa trị I và chlorine hóa trị I.
e) calcium, carbon và oxygenm biết calcium hóa trị II và nhóm nguyên tử CO3 có hóa trị II.
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
a) Công thức chung: FexCly
Theo quy tắc hóa trị: x.III = y.I
Lấy x = 1, y = 3 hợp chất là FeCl3: iron(III) chloride.
b) Công thức chung: NaxOy
Theo quy tắc hóa trị: x.I = y.II
Lấy x = 2, y = 1 hợp chất là Na2O: sodium oxide.
c) Công thức chung: HxFy
Theo quy tắc hóa trị: x.I = y.I
Lấy x = 1, y = 1 hợp chất là HF: hydrogen fluorine.
d) Công thức chung: KxCly
Theo quy tắc hóa trị: x.I = y.I
Lấy x = 1, y = 1 hợp chất là KCl: potassium chloride.
e) Công thức chung: Cax(CO3)y
Theo quy tắc hóa trị: x.II = y.II
Lấy x = 1, y = 1 hợp chất là CaCO3: calcium carbonate.
Bài 7.10 trang 27 SBT KHTN lớp 7 - Kết nối tri thức
Sử dụng thông tin trong Bảng hóa trị thường gặp của một số nguyên tố hóa học (Bảng 7.2 trang 43 SGK), hãy viết công thức hóa học của:
a) copper (I) oxide, (hợp chất hai nguyên tố giữa Cu và O, trong đó Cu hóa trị I).
b) zinc phosphate (hợp chất chứa Zn liên kết với nhóm nguyên tử PO4).
c) calcium carbonate (hợp chất chứa Ca liên kết với nhóm nguyên tử CO3).
d) sodium hydroxide (hợp chất chứa Na liên kết với nhóm nguyên tử OH).
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
a) Oxygen có hóa trị II.
Công thức chung: CuxOy
Theo quy tắc hóa trị: x.I = y.II
Lấy x = 2, y = 1 hợp chất copper(I) oxide có công thức là Cu2O.
b) Zinc có hóa trị II, nhóm PO4 có hóa trị III.
Công thức chung: Znx(PO4)y.
Theo quy tắc hóa trị: x.II = y.III
Lấy x = 3, y = 2 hợp chất zincphosphate: Zn3(PO4)2.
c) Calcium có hóa trị II, nhóm CO3 có hóa trị II.
Công thức chung: Cax(CO3)y.
Theo quy tắc hóa trị: x.II = y.II
Lấy x = 1, y = 1 hợp chất calcium carbonate: CaCO3.
d) Sodium có hóa trị I, nhóm OH có hóa trị I.
Công thức chung: Nax(OH)y.
Theo quy tắc hóa trị: x.I = y.I
Lấy x = 1, y = 1 hợp chất sodium hydroxide: NaOH.
Bài 7.11 trang 27 SBT KHTN lớp 7 - Kết nối tri thức
Hãy tính hóa trị của đồng và sắt trong các hợp chất sau: Cu(OH)2, Fe(NO3)3.
(Biết hóa trị của nhóm OH là I và của nhóm NO3 là I).
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
Xét hợp chất Cu(OH)2, gọi hóa trị của Cu là x ta có: x.1 = I.2 ⇒ x = II.
Vậy trong Cu(OH)2 hóa trị của Cu là II.
Xét hợp chất Fe(NO3)3, gọi hóa trị của Fe là y ta có: y.I = I.3 ⇒ y = III.
Vậy hóa trị của Fe trong Fe(NO3)3 là III.
Bài 7.12 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Chọn câu trả lời đúng:
A. Hợp chất ammonia có công thức hóa học là NH4.
B. Hợp chất carbon monooxide có công thức hóa học là CO2.
C. Hợp chất iron (III) oxide có công thức hóa học là Fe3O2.
D. Hợp chất zinc oxide có công thức hóa học là ZnO.
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
Đáp án đúng là: D
A sai vì ammonia: NH3.
B sai vì carbon monoxide: CO.
C sai vì iron(III) oxide: Fe2O3.
Bài 7.13 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Cho biết công thức hóa học của hợp chất được tạo bởi hai nguyên tố X và O (oxygen); Y và H (hydrogen) lần lượt là XO và YH3.
Hãy lập công thức hóa học của hợp chất giữa X với Y, biết X và Y có hóa trị bằng hóa trị của chúng trong các hợp chất XO và YH3.
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
Lời giải:
ì công thức hóa học của hợp chất tạo bởi X và O là XO nên X có hóa trị II. Hợp chất của Y với H là YH3 nên Y có hóa trị III.
Gọi công thức hóa học của hợp chất giữa X và Y là: XaYb.
Áp dụng quy tắc hóa trị: a.II = b.III
Chọn a = 3, b = 2, công thức hóa học của hợp chất giữa X và Y là: X3Y2.
Bài 7.14 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Lập công thức hóa học và tính khối lượng phân tử của hợp chất được tạo thành bởi:
a) K và Cl, Ba và Cl, Al và Cl.
b) K và nhóm SO4, Ba và nhóm SO4, Al và nhóm SO4.
(Biết khối lượng nguyên tử của K = 39; Cl = 35,5; Ba = 137; Cl = 27; S = 32; O = 16).
Phương pháp:
- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
- Khối lượng phân tử AxBy
\({{\rm{M}}_{{{\rm{A}}_{\rm{x}}}{{\rm{B}}_{\rm{y}}}}}{\rm{ = x }}{\rm{. }}{{\rm{M}}_{\rm{A}}}{\rm{ + y }}{\rm{. }}{{\rm{M}}_{\rm{B}}}\)
Lời giải:
Cách nhầm nhanh công thức hóa học khi biết hóa trị:
Cách nhầm nhanh: x = b; y = a. Chọn cặp x : y nhỏ nhất.
a) Công thức hóa học KCl.
Khối lượng phân tử: 39 + 35,5 = 74,5 (amu).
Công thức hóa học BaCl2.
Khối lượng phân tử: 137 + 35,5.2 = 208 (amu).
Công thức hóa học AlCl3.
Khối lượng phân tử: 27 + 35,5.3 = 133,5 (amu).
b) Công thức hóa học K2SO4.
Khối lượng phân tử: 39.2 + 32 + 16.4 = 174 (amu).
Công thức hóa học BaSO4.
Khối lượng phân tử: 137 + 32 + 16.4 = 233 (amu).
Công thức hóa học: Al2(SO4)3.
Khối lượng phân tử: 27.2 + (32 + 16.4).3 = 342 (amu).
Bài 7.15 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Xác định thành phần phần trăm của các nguyên tố trong các hợp chất sau:
a) Si và O trong hợp chất SiO2 (là thành phần chính của thủy tinh).
b) Na và Cl trong hợp chất NaCl (muối ăn).
(Biết khối lượng nguyên tử của Si = 28; O = 16; Na = 23; Cl = 35,5).
Phương pháp:
- Khối lượng phân tử của một chất bằng tổng khối lượng của các nguyên tử trong phân tử khối của chất đó.
Đơn vị: amu.
Lời giải:
a) Khối lượng phân tử của SiO2 là: 28 + 16.2 = 60 (amu).
Phần trăm khối lượng các nguyên tố trong hợp chất:
b) Khối lượng phân tử NaCl là: 23 + 35,5 = 58,5 (amu).
Phần trăm khối lượng các nguyên tố trong hợp chất:
Bài 7.16 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Tỉ lệ khối lượng giữa hai nguyên tố carbon và hydrogen trong hợp chất methan luôn không đổi là 3 : 1. Hãy lập công thức hóa học của khí methane, biết khối lượng nguyên tử của C = 12; H = 1.
Phương pháp:
- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.
- Có thể tìm công thức hóa học của hợp chất bằng cách tìm chỉ số nguyên tối giản của các nguyên tử trong hợp chất.
Lời giải:
Gọi công thức hóa học của khí methane là CxHy, ta có:
Vậy công thức hóa học của khí methane là: CH4.
Bài 7.17 trang 28 SBT KHTN lớp 7 - Kết nối tri thức
Nguyên tử của các nguyên tố X, Y và Z lần lượt có 8, 17 và 11 electron. Nguyên tử neon và argon lần lượt có 10 và 18 electron.
a) Xác định công thức hóa học của hợp chất được tạo thành từ các nguyên tử của các nguyên tố sau:
(i) X và Z (ii) Y và Z (iii) X với X.
b) Kiểu liên kết hóa học giữa các nguyên tử trong các hợp chất trên là liên kết gì?
c) Dự đoán hai tính chất của hợp chất được tạo thành trong trường hợp a(i) và a(ii).
Lời giải:
a) Nguyên tố X có Z = 8, thuộc nhóm VIA, là phi kim; nguyên tố Y có Z = 17, thuộc nhóm VIIA, là phi kim; nguyên tố Z có Z = 11, thuộc nhóm IA là kim loại. Công thức hóa học của các hợp chất tạo thành từ nguyên tử các nguyên tố:
(i) X và Z:
X thiếu 2 electron so với khí hiếm Ne; Z hơn 1 electron so với khí hiếm Ne. Do đó 2 nguyên tử Z nhường 2 electron cho 1 nguyên tử X. Công thức hóa học là Z2X (quy ước viết kim loại trước phi kim).
(ii) Y và Z:
Y thiếu 1 electron so với khí hiếm Ar; Z thừa 1 electron so với khí hiếm Ne. Do đó 1 nguyên tử Z nhường 1 electron cho nguyên tử Y. Công thức hóa học là ZY.
(iii) X với X: Đơn chất giữa hai nguyên tử X có công thức hóa học là X2.
b) Kiểu liên kết hóa học giữa các nguyên tử trong Z2X: liên kết ion; ZY: liên kết ion; trong X2: liên kết cộng hóa trị.
c) Hai tính chất của các hợp chất ion ZX2 và ZY: là chất rắn, tan trong nước, có nhiệt độ nóng chảy cao.
Sachbaitap.com
Bài viết liên quan
Các bài khác cùng chuyên mục
- Giải SBT KHTN 7 Kết nối tri thức bài 24 trang 57, 58, 59 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 23 trang 56, 57 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 22 trang 54, 55 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 21 trang 53, 54 (15/12)
- Giải SBT KHTN 7 Kết nối tri thức bài 20 trang 51, 52 (10/12)
- Bài 24. Thực hành: Chứng minh quang hợp ở cây xanh
- Bài 23. Một số yếu tố ảnh hưởng đến quang hợp
- Bài 22. Quang hợp ở thực vật
- Bài 21. Khái quát về trao đổi chất và chuyển hóa năng lượng
- Chương VII. Trao đổi chất và chuyển hóa năng lượng sinh vật
- Bài 20. Chế tạo nam châm điện đơn giản
- Bài 19. Từ trường
- Bài 18. Nam châm
- Chương VI. Từ
- Bài 17. Ảnh của vật qua gương phẳng
- Bài 22 Đọc mở rộng trang 111 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 22 Luyện viết đoạn văn thể hiện tình cảm, cảm xúc về một sự việc trang 111 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 22 Bộ đội về làng trang 109 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Viết đoạn văn nêu ý kiến tán thành một sự việc, hiện tượng (Bài viết số 2) trang 108 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Luyện tập về câu ghép trang 107 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 21 Anh hùng lao động Trần Đại Nghĩa trang 106 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Đền ơn đáp nghĩa trang 104 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Đánh giá, chỉnh sửa đoạn văn nêu ý kiến tán thành một sự vật, hiện tượng trang 103 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 20 Cụ Đồ Chiểu trang 101 SGK Tiếng Việt 5 Kết nối tri thức tập 2
- Bài 19 Viết đoạn văn nêu ý kiến tán thành một sự việc, hiện tượng (Bài viết số 1) trang 100 SGK Tiếng Việt 5 Kết nối tri thức tập 2
 Tải app loigiaihay.com cho Android để lưu và xem mà không cần mạng!
Tải app loigiaihay.com cho Android để lưu và xem mà không cần mạng!